北京百普赛斯生物科技股份有限公司品牌商
14 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
IL-2药物开发策略解读篇:联合疗法
1023 人阅读发布时间:2026-02-12 17:33
白细胞介素-2(IL-2)是免疫治疗的经典靶点,凭借激活效应免疫细胞、调控免疫稳态的作用,一直是研发热点。此前我们已解读过药物修饰、偏向性调节两大IL-2开发策略,二者均有效改善了传统IL-2毒性大、半衰期短的问题。但肿瘤免疫微环境复杂、肿瘤易发生免疫逃逸,单一疗法仍难以取得突破性疗效。因此,以“协同增效、优势互补”为核心的联合用药,或为突破 IL-2 治疗瓶颈、拓展免疫治疗应用的关键,也开启了IL-2 研发的“组合拳”时代。本期,我们将聚焦IL-2联合用药策略,看这把“免疫双刃剑”如何在联合疗法中展现价值。

联合用药核心逻辑:打破局限,实现1+1>2的免疫增效
IL-2疗法联合多种治疗策略旨在弥补单一IL-2疗法的短板,通过协同调节免疫系统的多个成分或靶向特定信号通路来最小化其不良反应。目前,IL-2联合用药已形成多条成熟研发路径,其中联合免疫检查点抑制剂、细胞疗法(如CAR-T)、化疗/靶向治疗,已形成较为清晰的研发路径,并在临床研究中展现出显著潜力。
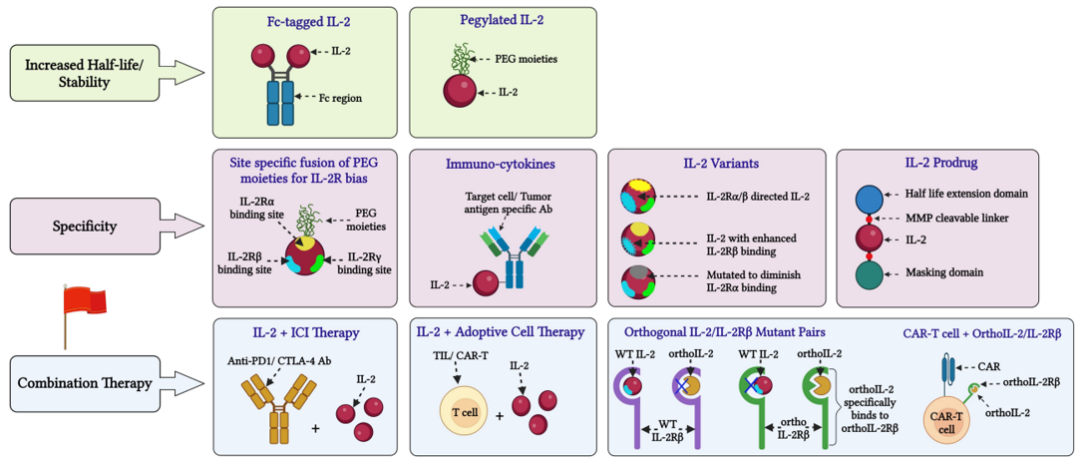
基于IL-2的免疫治疗新方法
主流联合策略进展盘点
IL-2联合免疫检查点抑制剂:“激活+解锁”协同增效
免疫检查点是维持免疫稳态的关键负调控因子。已获批的PD-1/PD-L1或CTLA-4抑制剂虽能“解锁”T细胞功能,但在部分“免疫冷”肿瘤(如微卫星稳定型结直肠癌、胰腺癌)中单药疗效有限,客观缓解率(ORR)常低于10%。IL-2可直接促进T细胞增殖与活化,二者联用形成“激活+解锁”的协同效应。临床前研究显示,该组合或能逆转T细胞耗竭,增强抗肿瘤活性。
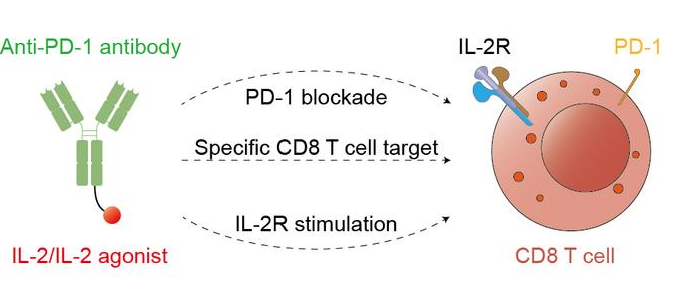
PD-1/IL-2双功能分子可阻断PD-1介导的免疫抑制信号,同时顺式激活T细胞
PD-1/IL-2双功能分子可阻断PD-1介导的免疫抑制信号,同时顺式激活T细胞,成为联合治疗的重要探索方向。2025年11月18日,iLeukon Therapeutics的脂质体mRNA IL2v产品ILKN421H获FDA再生医学先进疗法(RMAT)与快速通道(FTD)双重认定,加速其与帕博利珠单抗联合用于晚期非小细胞肺癌(NSCLC)一线治疗的研发。SITC年会公布的I期数据显示,20例一线NSCLC患者联合用药确认ORR达80%,PD-L1阳性患者ORR升至87%,中位PFS预计超12个月。该突破源于IL-2疗法的颠覆性重构,以“精准免疫激活”为核心,为免疫治疗耐药难题提供新路径,目前其II期临床已获FDA批准,进一步评估联合疗法疗效。
化疗药物能直接杀伤肿瘤细胞并释放肿瘤相关抗原,但可能同时抑制免疫系统并诱发耐药。IL-2与化疗联用,旨在结合直接的细胞毒作用与系统性的免疫激活,有望提升疗效、逆转耐药并拓宽受益人群。IL-2可激活效应免疫细胞,帮助清除化疗后残留病灶,降低复发风险。

2025年ESMO Asia大会公布的PICM研究提供了有力证据。该研究在免疫耐药的微卫星稳定/错配修复完整(MSS/pMMR)局部进展期直肠癌(LARC)患者中,探索了以IL-2为核心的“去放疗”联合方案(含PD-1抑制剂及化疗)。结果显示,病理完全缓解(pCR)率从标准治疗的17.6%显著提升至52.0%,且所有患者均实现R0切除。机制上,IL-2有助于激活肿瘤微环境中的T细胞和NK细胞,将“冷肿瘤”转化为“热肿瘤”,与化疗及免疫检查点抑制剂产生协同。该方案避免放疗相关损伤,有利于器官功能保留,支持“观察与等待”策略的实施。此前一项单臂研究(NCT06108596)已提示该策略的pCR率达42.4%,初步验证了IL-2的协同增效作用。
CAR-T细胞疗法在实体瘤中面临细胞持久性差、易耗竭和肿瘤浸润不足等挑战。IL-2作为关键的T细胞生长因子,可与CAR-T疗法联用以改善这些瓶颈。其协同机制在于:CAR-T细胞提供特异性靶向杀伤,而IL-2可支持CAR-T细胞的体外扩增、延长其在体内的存活时间、抑制耗竭相关分子表达,并同时激活内源性免疫细胞,形成双重杀伤效应。
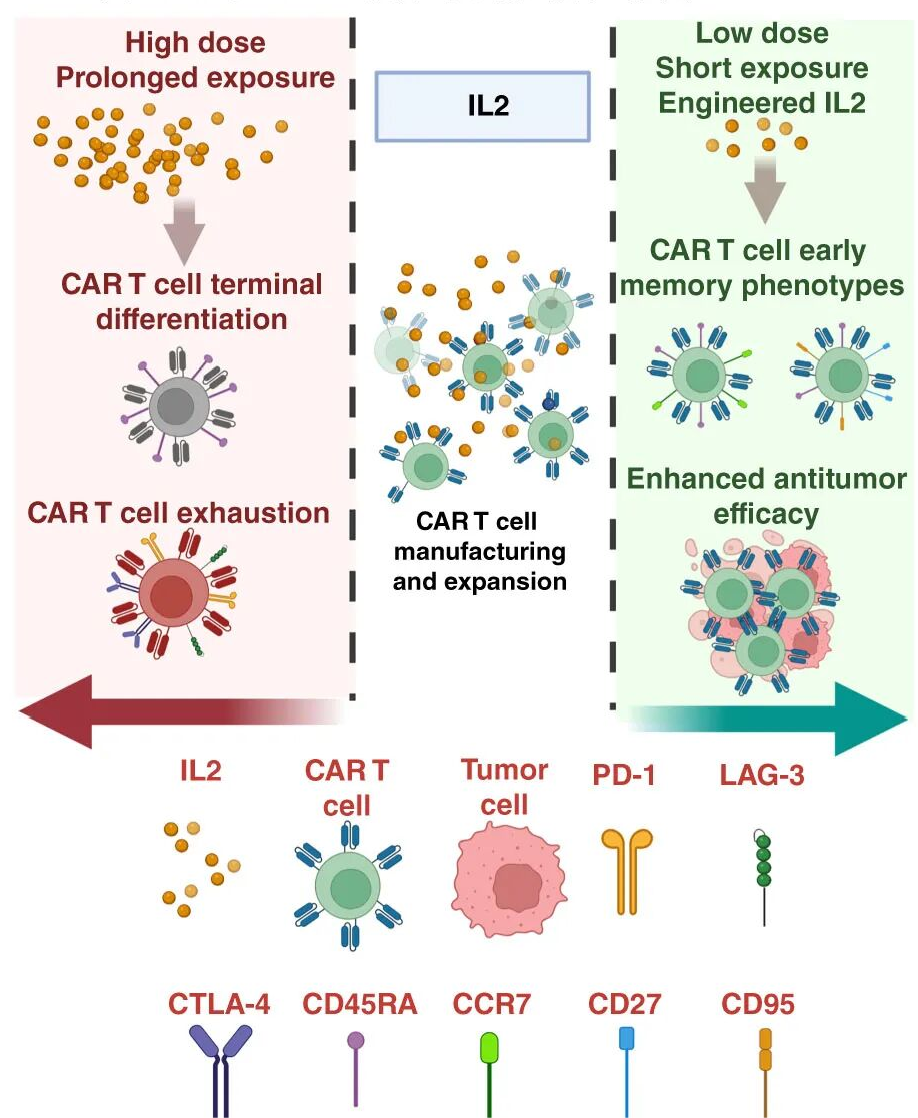
IL-2在CAR-T治疗中的多效性应用
Imugene Limited公司的一项研究入选2025年美国血液学会(ASH)年会摘要。该研究评估了同种异体CD19 CAR-T细胞(Azer-cel)联合低剂量IL-2,在既往接受过自体CD19 CAR-T治疗失败的弥漫大B细胞淋巴瘤(LBCL)患者中的疗效。初步数据显示,联合疗法展现出积极的临床活性、持久的CAR-T细胞扩增迹象以及可管理的安全性,支持该方案的进一步开发。
IL-2联合用药虽具巨大潜力,但仍面临挑战:联合方案优化不足,药物联合比例、给药顺序和剂量需更多临床试验探索;肿瘤异质性导致疗效存在个体差异,难以实现“一刀切”;多药物联合可能增加不良反应,需平衡疗效与安全性。随着药物修饰、偏向性调节技术的成熟及对肿瘤免疫微环境的深入理解,更多联合方案将进入临床试验、走向临床应用,有望在多类疾病中实现突破,为患者带来更高效安全的治疗选择。ACROBiosystems百普赛斯开发了系列IL-2及其受体蛋白:IL-2,IL-2Rα,IL-2Rβ,IL-2Rγ,IL-2Rβγ异源二聚体蛋白,以及IL-2Rαβγ异源三聚体蛋白,助力IL-2在联合用药、药物修饰、偏向性调节等创新策略中的开发应用,为免疫治疗保驾护航。

- 亲和力经SPR验证
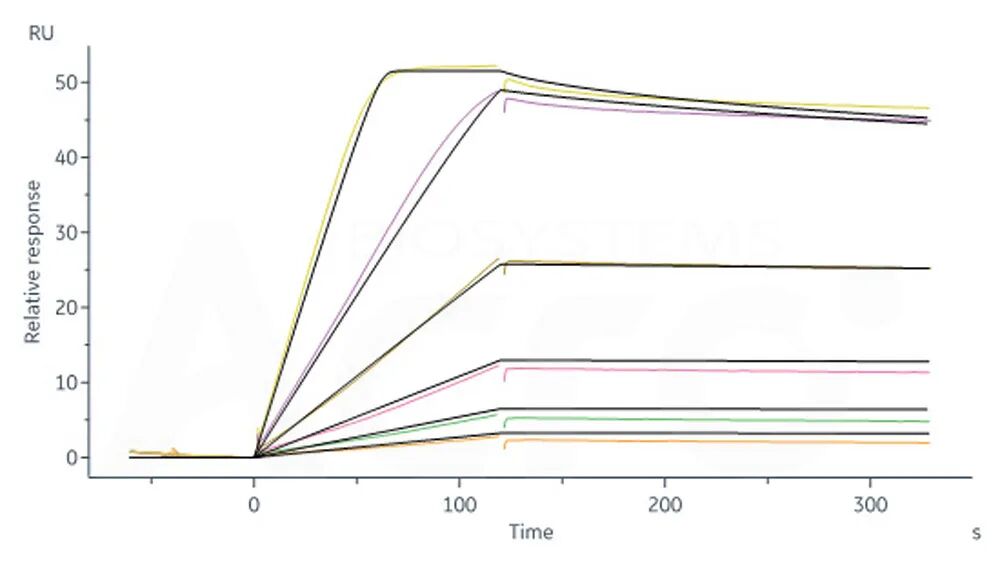
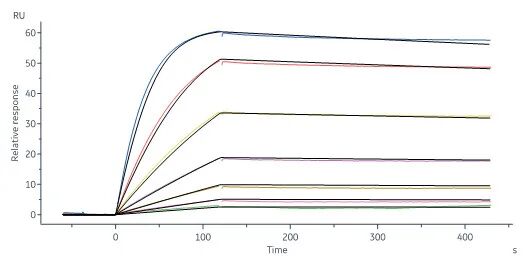
- 高生物活性经ELISA验证
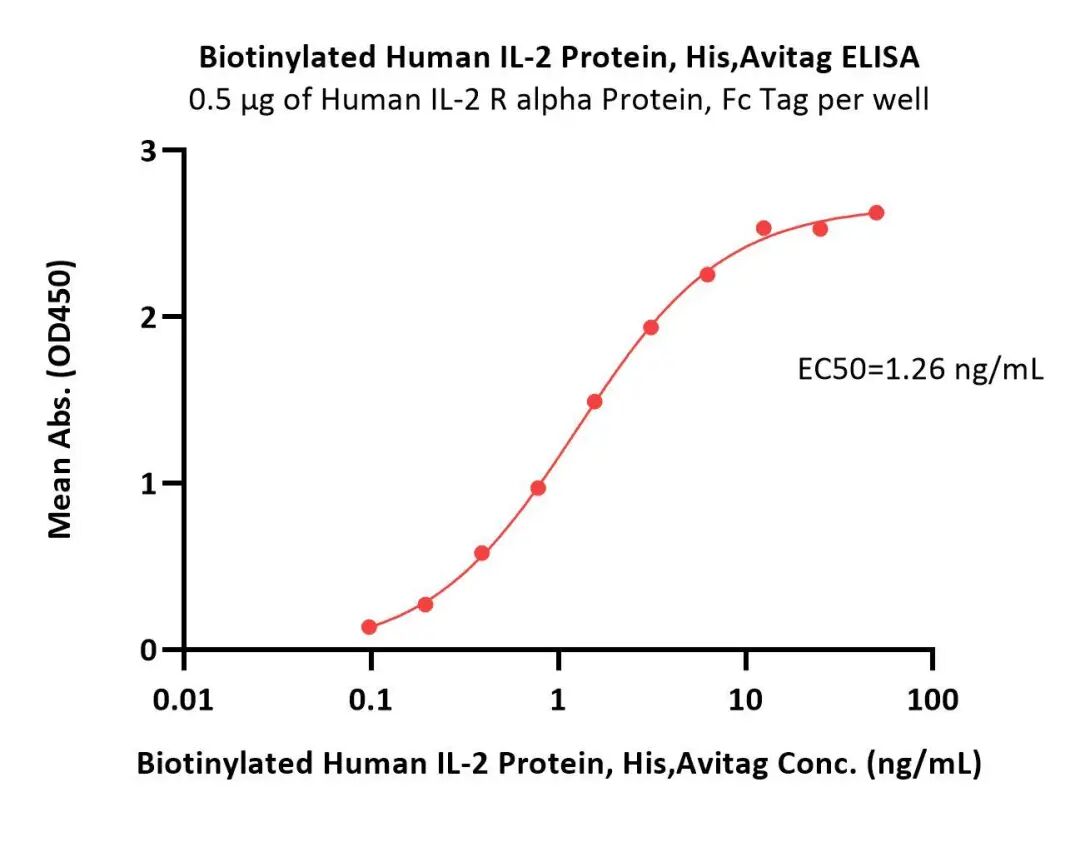
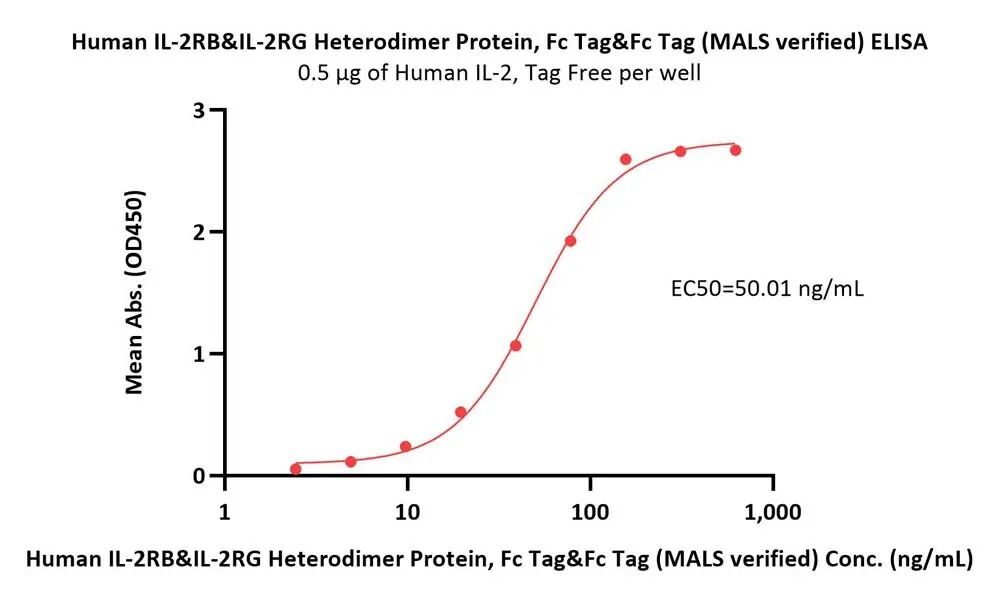
Immobilized Human IL-2 Protein, premium grade (Cat. No. IL2-H5215) at 5 μg/mL (100 μL/well) can bind Human IL-2RB&IL-2RG Heterodimer Protein, Fc Tag&Fc Tag (MALS verified) (Cat. No. ILG-H5254) with a linear range of 2-156 ng/mL (QC tested).
参考文献
1. Rokade S, Damani A M, Oft M, et al. IL-2 based cancer immunotherapies: an evolving paradigm[J]. Frontiers in Immunology, 2024, 15: 1433989.
2. Balkhi S, Bilato G, De Lerma Barbaro A, et al. Efficacy of anti-cancer immune responses elicited using tumor-targeted IL-2 cytokine and its derivatives in combined preclinical therapies[J]. Vaccines, 2025, 13(1): 69.
3. West E E, Jin H T, Rasheed A U, et al. PD-L1 blockade synergizes with IL-2 therapy in reinvigorating exhausted T cells[J]. The Journal of clinical investigation, 2013, 123(6): 2604-2615.
4. Stewart C M, Siegler E L, Kenderian S S. The Pleiotropic Roles of Cytokines in Chimeric Antigen Receptor T-cell Therapy[J]. Cancer immunology research, 2026, 14(1): 10-21.
5. Pavy A, Sailer C, McSain S, et al. IL-2 mutein-mediated improvement of CAR T function in Relapsed/Refractory diffuse B cell lymphoma[J]. Blood, 2025, 146: 5880.
6. Stewart C M, Siegler E L, Kenderian S S. The Pleiotropic Roles of Cytokines in Chimeric Antigen Receptor T-cell Therapy[J]. Cancer immunology research, 2026, 14(1): 10-21.
7. 医麦客公众号
8. 佰傲谷公众号

ACROBiosystems
inquiry@acrobiosystems.com
15117918562
(备注:姓名+公司)



