北京百普赛斯生物科技股份有限公司品牌商
14 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
【靶点新势力】趋化因子及其受体的作用和免疫治疗策略
7066 人阅读发布时间:2022-06-09 16:48
趋化因子(chemokines)也称为趋化性细胞因子(chemotactic cytokines) ,是一组与其细胞表面受体一起发挥作用的、导致白细胞定向迁移的因子,由炎症细胞因子、生长因子和致病刺激诱导产生。趋化因子信号转导导致靶基因的转录,涉及细胞侵袭、运动、与细胞外基质(ECM)的相互作用和生存。趋化因子信号可以协调炎症过程中细胞的运动,以及造血干细胞、淋巴细胞和树突状细胞的稳态运输,还可能控制其他类型细胞的运动,如成体干细胞和内皮细胞。表达量适当的趋化因子受体细胞沿配体的化学梯度发生定向迁移(称为趋化因子梯度),使得细胞向高局部浓度的趋化因子移动。
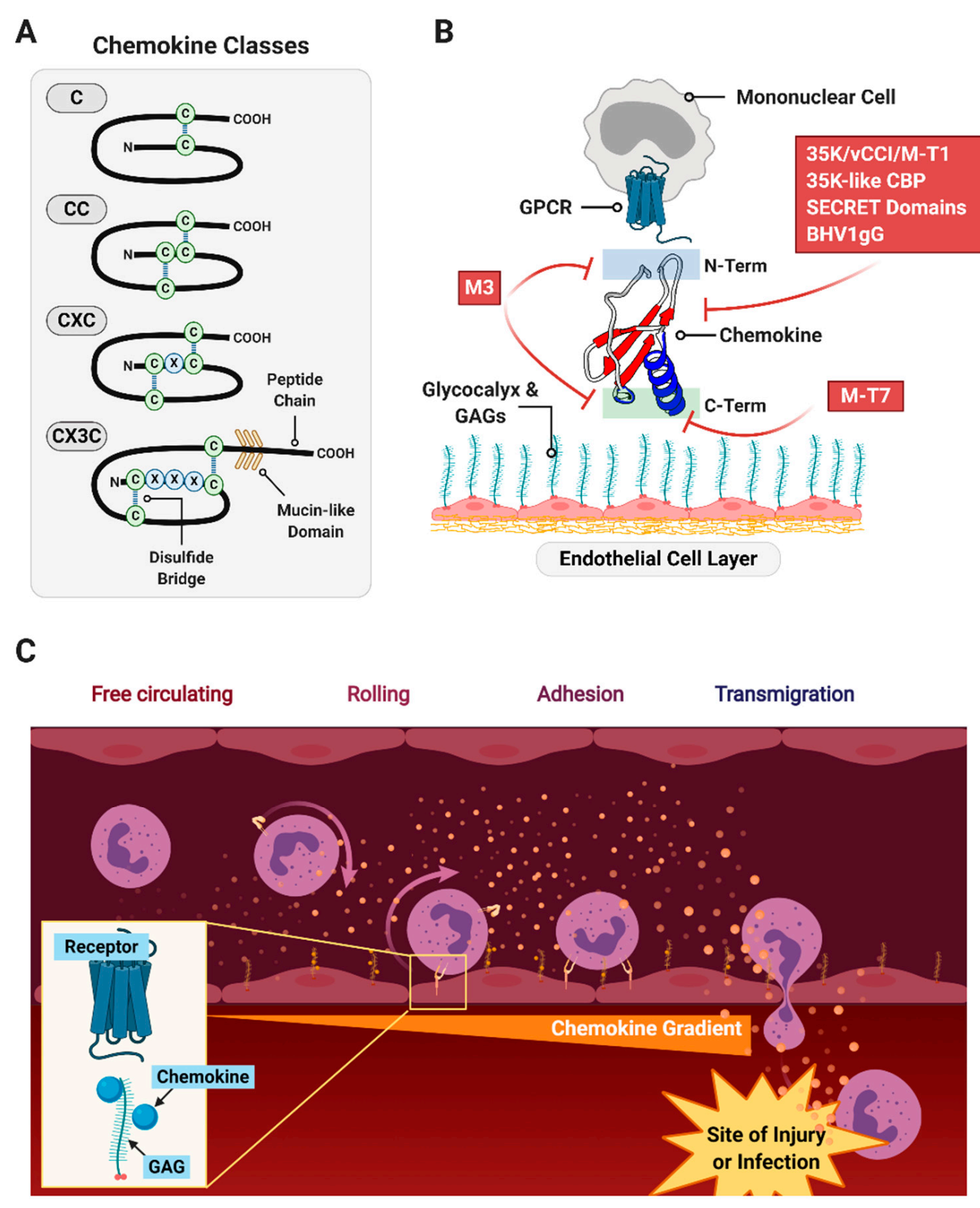
趋化因子及其受体的分类和作用
趋化因子系统是随着脊椎动物进化而来的,人类有近50个基因编码趋化因子配体,20多个对应的人类趋化因子受体基因,是七次跨膜G蛋白偶联受体(GPCRs)。根据前两个与氨基端相邻的半胱氨酸的位置,趋化因子被分为四类,CXC、CC、CX3C或C,受体命名基本上遵循趋化因子的命名,即CC趋化因子与CC趋化因子受体结合,CXC配体与CXC受体结合。
趋化因子与其受体具有交叉作用,一个趋化因子可与多个趋化因子受体结合,一个受体也可以有多个高亲和的趋化因子。
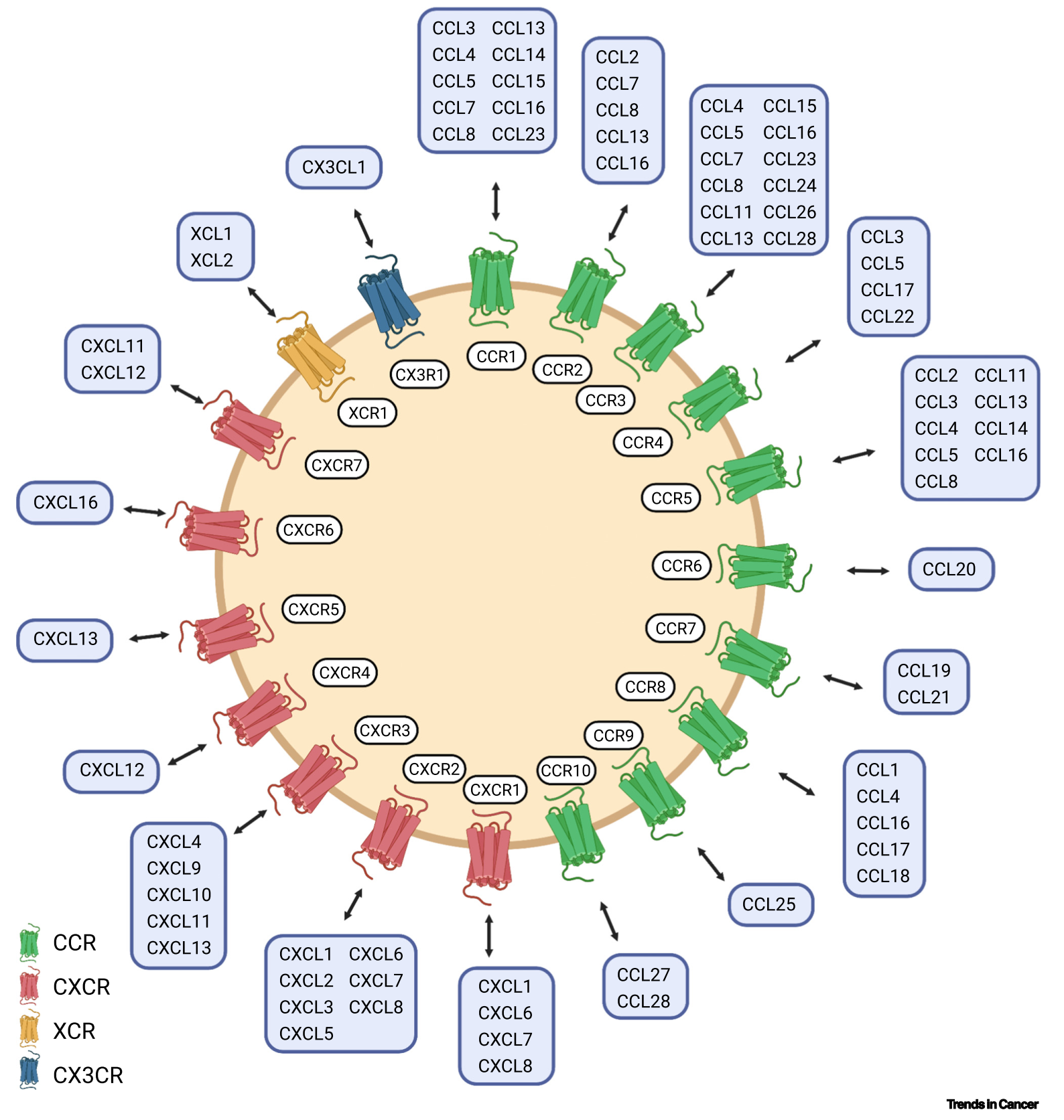
趋化因子及其受体的对应关系
趋化因子与其受体的相互作用调控免疫细胞在循环系统和组织器官间定向迁移,使免疫细胞到达感染、创伤和异常增殖部位,执行清除感染源、促进创伤愈合和消灭异常增殖细胞、维持组织细胞平衡的功能。
趋化因子及其受体在癌症中的作用
趋化因子在炎症和免疫中起关键作用,也是癌症相关炎症的关键介质,它们能够直接影响癌细胞的增殖和转移,具体作用如下:☞ 白细胞募集 — 免疫细胞的正确运动是由趋化因子空间和时间上的表达来协调的。炎性CC(CCL2、CCL3、CCL5)和CXC(CXCL1、CXCL2、CXCL5、CXCL6和CXCL8)趋化因子在肿瘤部位募集CCR2+单核细胞和CXCR2+中性粒细胞,分化为肿瘤相关巨噬细胞(TAM)和肿瘤相关中性粒细胞(TAN),发挥促肿瘤或抗肿瘤作用。一些存在于肿瘤部位的趋化因子可以改变白细胞的激活,例如作用于CXCR6的CXCL16在实体瘤中诱导巨噬细胞向亲肿瘤表型极化。CXCL9和CXCL10通过募集NK细胞、CD4+Th1和CD8+细胞毒性淋巴细胞而与Th1免疫反应密切相关,这可以引发抗肿瘤反应。此外,CCL20、CCL5和CXCL12是树突状细胞的有效引诱剂;CCL21和CCL19不仅招募CCR7+DC,而且还招募调节性T细胞(Tregs)。CCL17和CCL22作用于CCR4可以直接募集Tregs和Th2淋巴细胞,促进肿瘤生长和增殖。
☞ 血管生成 — CC和CXC趋化因子在肿瘤血管生成中发挥重要作用,对肿瘤生长和转移扩散至关重要。基于N-末端谷氨酸-亮氨酸-精氨酸(ELR)基序的存在,CXC趋化因子可分为具有血管生成作用的ELR+趋化因子和具有血管抑制作用的ELR-趋化因子。CCL2、CCL11、CCL16、CCL18和CXCL8促进肿瘤血管生成和内皮细胞存活。此外,CXCL16与CXCR6相互作用,是一种有效的血管生成介质。CXCL12和CCL2可通过分别直接结合肿瘤血管上表达的受体CXCR4和CCR2,或间接促进白细胞募集来促进血管生成和抑制内皮细胞的凋亡。相反,趋化因子,如CCL21和ELR-趋化因子(CXCL4、CXCL9、CXCL10和CXCL11)抑制血管生成和内皮细胞增殖。
☞ 肿瘤的生长和增殖 — 肿瘤自身产生的趋化因子通过与肿瘤细胞临时表达的趋化因子受体结合,直接促进癌细胞的增殖,激活不同的信号通路,如PI3K/AKT/NF-kB和MAPK/ERK通路。此外,它们还可以通过阻止肿瘤细胞的凋亡和调节促凋亡和抗凋亡分子之间的平衡(例如下调Bcl-2的表达或抑制caspase-3和caspase-9的激活)来促进肿瘤细胞的存活。
☞ 转移 — 癌细胞表达的趋化因子受体促进其向转移部位的迁移。参与这一现象的趋化因子和趋化因子受体有几种:CCR7介导肿瘤细胞向淋巴结的迁移,在那里产生其配体CCL19和CCL21;CCR10/CCL27轴促进黑色素瘤细胞在转移扩散过程中的黏附和存活;CCL28通过MAPK/ERK通路促进乳腺癌生长和转移;趋化因子受体CXCR5及其配体CXCL13促进前列腺癌的骨转移。在一些肿瘤中,CXCR4的表达赋予癌细胞迁移和转移到分泌高水平CXCL12的器官的能力。
利用趋化因子及其受体的免疫治疗策略 趋化因子及其受体作为免疫细胞转运的介质,参与肿瘤发展的各个阶段,在肿瘤微环境的组成中发挥着重要作用,具有促肿瘤和抗肿瘤的双重作用。一般来说,在免疫治疗中使用趋化因子及其受体有两种方法:① 靶向原性趋化因子:利用或靶向趋化因子的多种策略已经建立起来,新的药物候选在临床试验中进行验证。
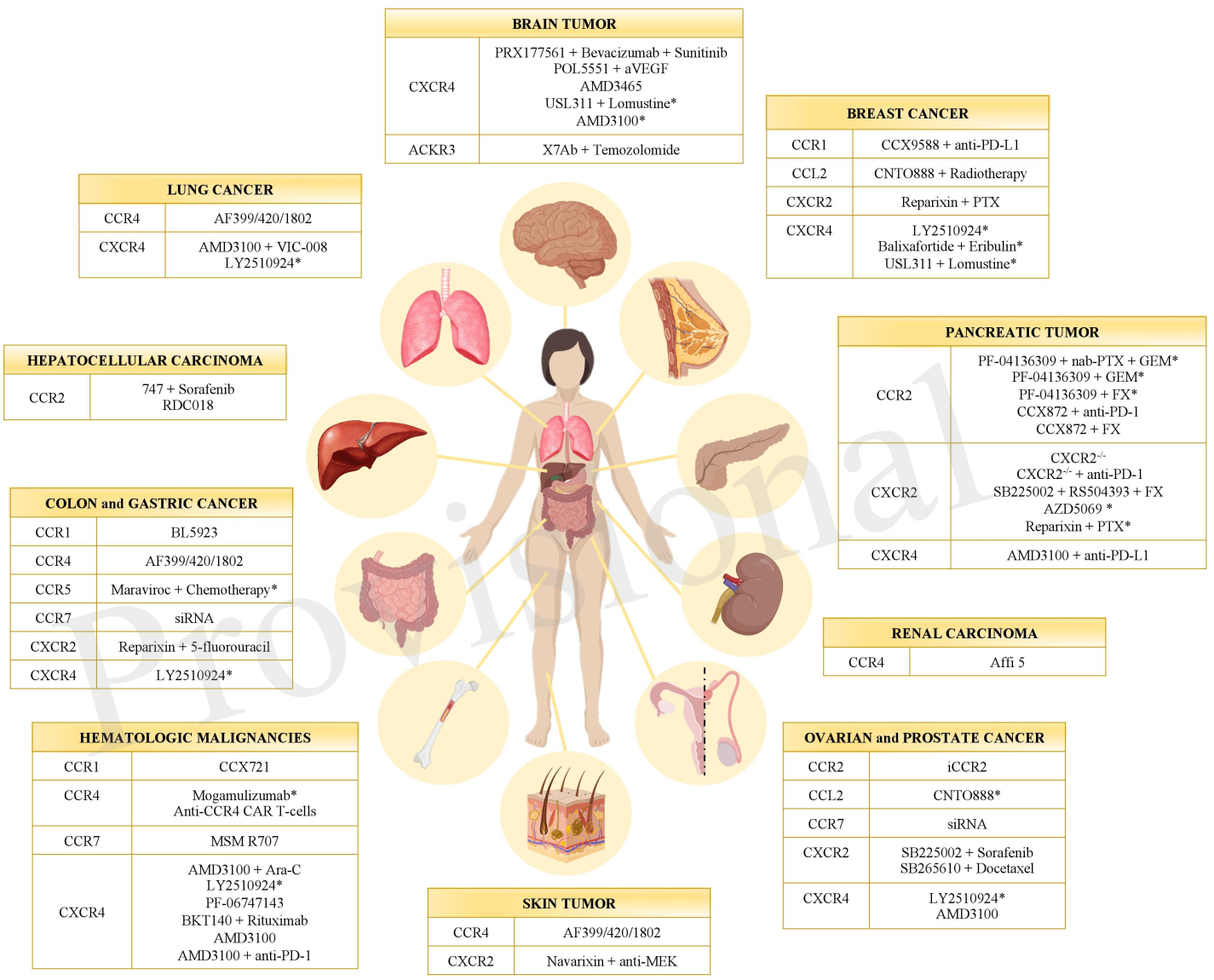
趋化因子及其受体参与癌症生物学作用与靶向药物
② 增加抗肿瘤趋化因子的浓度,作为单独治疗或与其他治疗策略结合,增强内源性效应细胞的招募和激活,从而介导有效的抗肿瘤免疫反应。目前,利用抗肿瘤趋化因子与癌症疫苗、溶瘤病毒(OVs)和CAR-T细胞疗法相结合的策略最近已经建立,现在正在临床I期和临床II期试验中探索。
利用抗肿瘤趋化因子的 结合治疗策略临床试验汇总
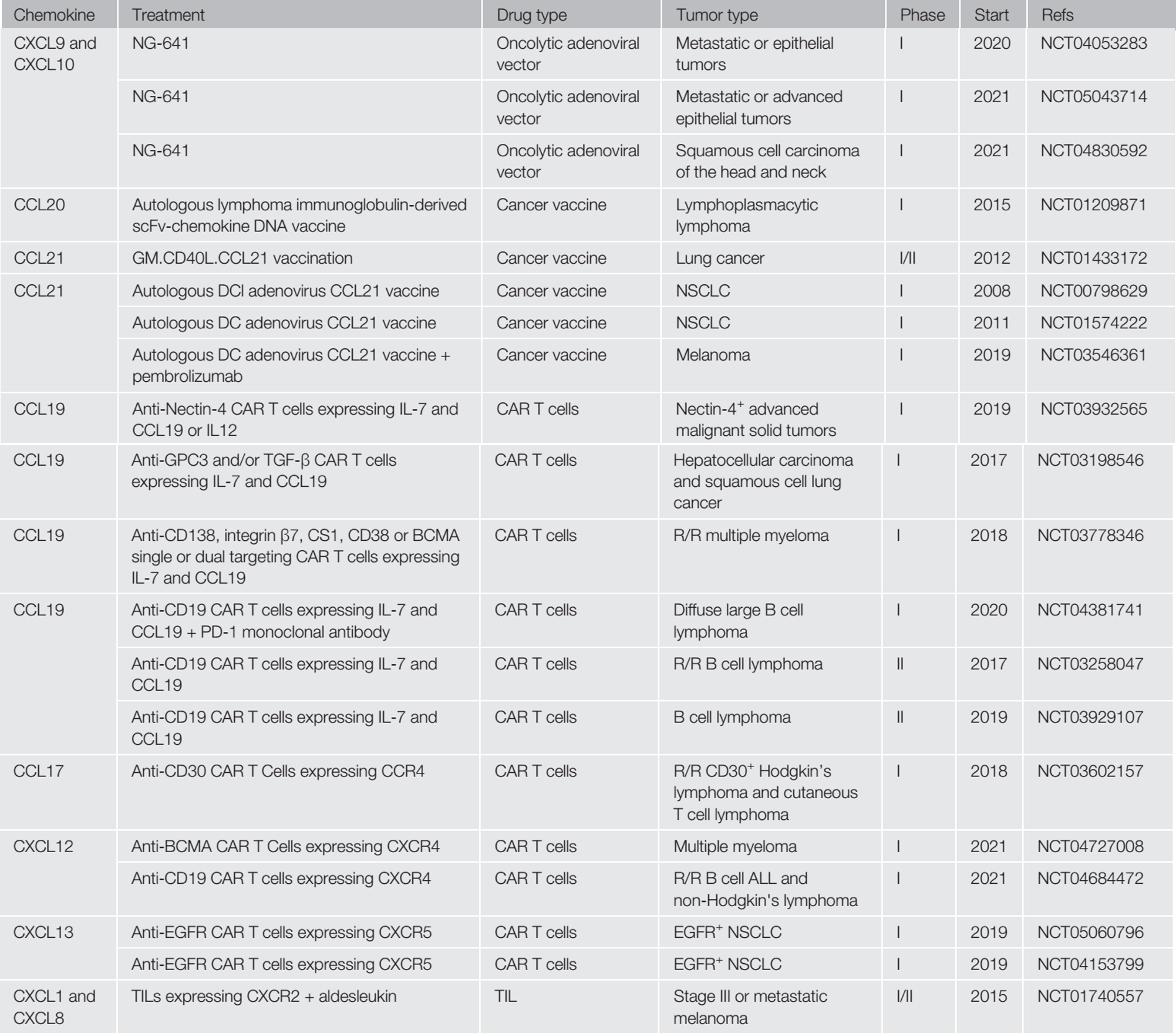
可以说,应用抗肿瘤治疗药物同时最大限度地利用趋化因子和白细胞介素调动内源性免疫细胞的策略是未来的一个强有力的策略。ACRO成功开发了一系列趋化因子及其受体,满足您的药物开发需要。
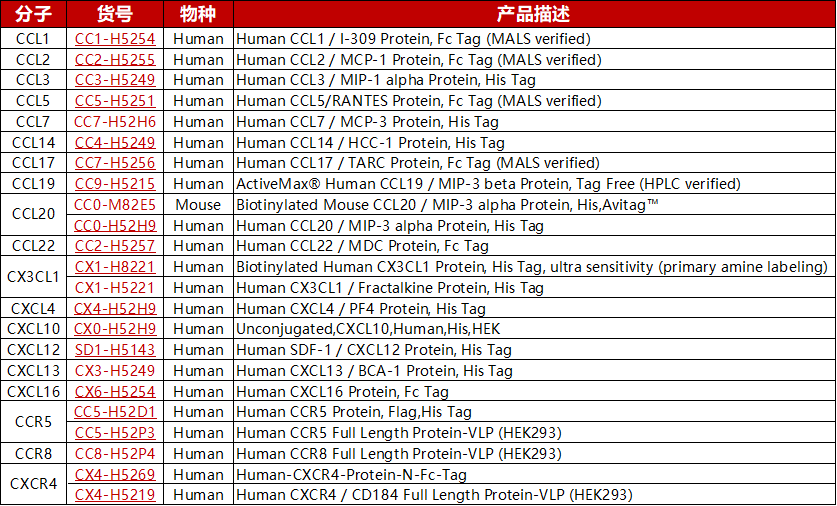
点击分子名称,查看更多产品信息及验证数据
免费申请protocol~
| CCL1 | CCL2 | CCL3 | CCL5 |
| CCL7 | CCL14 | CCL17 | CCL19 |
| CCL20 | CCL22 | CX3CL1 | CCL4 |
| CXCL10 | CXCL12 | CXCL13 | CXCL16 |
| CCR5 | CCR8 | CXCR4 | ... |
推荐阅读:
>>>【靶点新势力】趋化因子受体CCR5,抗 HIV的优秀靶点
ACROBiosystems秉承“从靶点蛋白开始,为更好生物医药” 的理念,开发了一系列包括白细胞介素(Interleukins)、生长因子(Growth Factors)、肿瘤坏死因子(TNFs)、趋化因子(Chemokines)、集落刺激因子(CSFs)、干扰素(IFNs)、补体因子等重组细胞因子及其受体蛋白产品,满足您的药物开发需求,与您共创靶向细胞因子的药物开发新篇章。

ACROBiosystems
inquiry@acrobiosystems.com
15117918562
(备注:姓名+公司)
参考文献:
1. Luster, A. D. Chemokines — Chemotactic Cytokines That Mediate Inflammation. New England Journal of Medicine (1998). DOI: 10.1056/NEJM199802123380706
2. Balkwill, F. Cancer and the chemokine network. Nature Reviews Cancer (2004). doi:10.1038/nrc1388
3. Bonecchi R, Mollica_poeta V, Capucetti A and Massara M. Chemokines and chemokine receptors: new targets for cancer immunotherapy. Front. Immunol. (2018). doi:10.3389/fimmu.2019.00379
4. Balkwill, F. R. The chemokine system and cancer. The Journal of Pathology (2011). DOI: 10.1002/path.3029
5. Yaron, J. R., Zhang, L., Guo, Q., Burgin, M., Schutz, L. N., Awo, E., … Lucas, A. R. Deriving Immune Modulating Drugs from Viruses—A New Class of Biologics. Journal of Clinical Medicine (2020). doi:10.3390/jcm9040972
6. Florian Märkl, Duc Huynh, Stefan Endres, Sebastian Kobold. Utilizing chemokines in cancer immunotherapy,Trends in Cancer (2022). https://doi.org/10.1016/j.trecan.2022.04.001




