北京百普赛斯生物科技股份有限公司品牌商
14 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
EP 2.6.7(12.2 版) 4 月强制生效!ACRO 全流程方案助力支原体检测 NAT 法落地无忧
675 人阅读发布时间:2026-03-07 16:33
2026 年 4 月 1 日,欧洲药典 EP 2.6.7(12.2 版)正式强制实施!这场支原体检测领域的监管变革,首次将 NAT(核酸扩增)法确立为与传统培养法、指示细胞法等效的核心检测方法,标志着生物药质控正式进入 “快检 + 精准” 双轨时代。面对新规对灵敏度、标准品、基质适配等的严苛要求,ACROBiosystems 百普赛斯支原体全流程检测方案,以支原体快速检测试剂盒(qPCR) (Cat. No. OPA-S102)和支原体DNA提取试剂盒(磁珠法) (Cat. No. OPA-E101)为核心,从法规适配、性能验证到场景覆盖全面超越行业标准,更贴合药企实际需求,让生物药 QC 轻松应对新规挑战!

EP 2.6.7章作为欧洲药典中支原体检测的核心章节,长期以来规定了培养法与指示细胞培养法的传统检测策略。随着qPCR、数字PCR等分子方法的成熟与广泛应用,EP修订委员会对该章节进行了全面重构,明确将NAT方法纳入主线框架,并与传统方法等效对待。这一变化不仅反映了当今微生物控制科学技术的发展,也体现了欧美、亚洲主要药典监管趋同的趋势。
新修订的EP 2.6.7并不单纯将NAT作为可选替代,而是提出了基于风险评估的检测策略:在未被单一专门章节或专论覆盖的情况下,检测方案可采用传统培养体系与NAT体系之一,但必须能够同时覆盖“可培养(culturable)”和“不可培养(non-culturable)”支原体。
EP 2.6.7(12.2 版)的修订并非简单新增方法,而是建立了一套完整的 NAT 法监管框架,每一项要求都直指检测可靠性与合规性。ACRO 现有支原体检测试剂不仅完全符合新规,更在关键指标上实现超规适配:
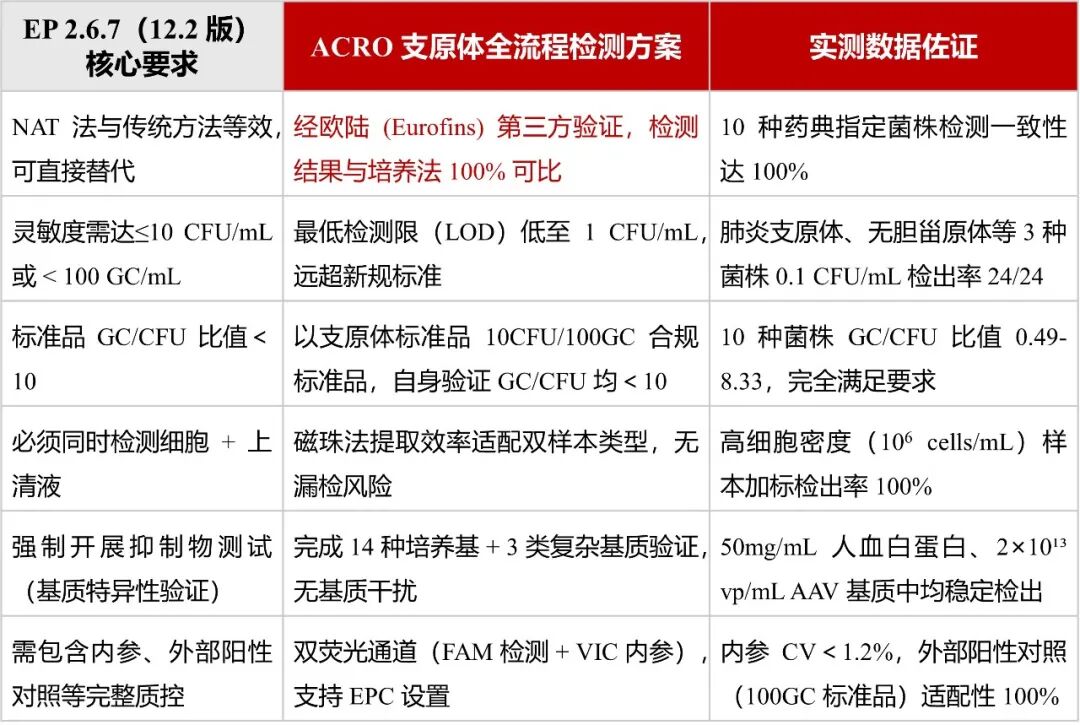

扫码申请欧陆第三方验证报告文档
-
覆盖 250 + 柔膜体纲物种,含 EP 指定全部 10 种核心菌株,10 CFU/mL 浓度下 24 次检测均为阳性,无假阴性;
-
与肺炎链球菌、E.coli、CHO/HEK293 细胞等近缘菌株 / 细胞系无交叉反应,特异性达 100%,避免误判风险。
新规特别关注 ATMP、病毒载体等复杂基质样品的检测可靠性,ACRO 方案针对性完成多重验证:
-
兼容高细胞密度(10⁶-10⁷ cells/mL)、10% DMSO 冻存液、含药培养基(Puro/Zeo/G418)等工业常用样品;
-
专项验证高滴度 AAV病毒(2×10¹³ vp/mL)、50mg/mL 人血白蛋白基质,加标后检出率 100%,Ct 值稳定无漂移,完美适配细胞/基因治疗、蛋白药等场景。
-
从样品提取到结果判读全程仅需 2 小时 45 分钟,远超同类产品 4-5 小时的检测周期,大幅提升批放行效率;
-
配套 OPE-32S 自动化核酸提取仪 + 96 孔深孔板耗材,支持高通量操作,减少人工误差。
-
提供完整的方法学验证报告,包含检测限、精密度、耐用性等 6 大维度数据;
-
可免费申请欧陆 (Eurofins) 一级验证文档,深度了解验证结果;
-
产品在符合 ISO 13485 标准厂区生产制造,每批次附完整 COA 报告,可追溯性强。
-
试剂盒 - 15~-30℃可稳定保存 18 个月,2-8℃冷藏 20 天性能无衰减;
-
经 15 次冻融循环后,Ct 值 CV<1.02%,无需担心反复使用导致的性能波动。
ACRO 支原体检测方案不仅适配新规要求,更覆盖生物药全生命周期质控节点,满足不同场景的检测需求:
-
原材料验证:胎牛血清、培养基、质粒等源头污染筛查;
-
过程控制:生物反应器扩增、细胞库传代等中间样品检测;
-
批次放行:单抗、细胞治疗产品、病毒载体等最终产品合规检测;
-
特殊场景:ATMP、基因治疗药物等复杂基质样品专项检测。
ACROBiosystems百普赛斯提供完善的支原体全流程检测方案,涵盖自动化核酸提取仪(Cat. No. OPE-32S)、支原体DNA提取试剂盒(Magnetic beads) (Cat. No. OPA-E101)、支原体快速检测试剂盒(qPCR) (Cat. No. OPA-S102)。该解决方案以 “法规精准适配 + 超规性能 + 场景全覆盖” 的核心优势,成为新规下的最优选择。现有试剂无需升级即可直接使用,让 QC 部门告别重复验证、避免生产延误。

为帮助药企快速完成方法转移与体系升级,ACRO 同步推出 “新规合规赋能计划”:
-
技术专家上门 DEMO 服务,现场演示复杂基质样品检测全流程;
-
针对细胞治疗、基因治疗等领域,提供定制化验证方案支持。
2026年 4 月新规生效进入倒计时,生物药企业合规刻不容缓!

扫码咨询
支原体快速检测试剂盒已通过欧陆(Eurofins)第三方机构全面验证,经验证其检测结果与培养法具有可比性,进一步证实了其检测的可靠性。为更好支持客户平台建立及药物申报,我们可为您提供完整的验证报告文档。

-
ACRO支原体全流程检测方案全面适配细胞治疗/基因治疗产品检测
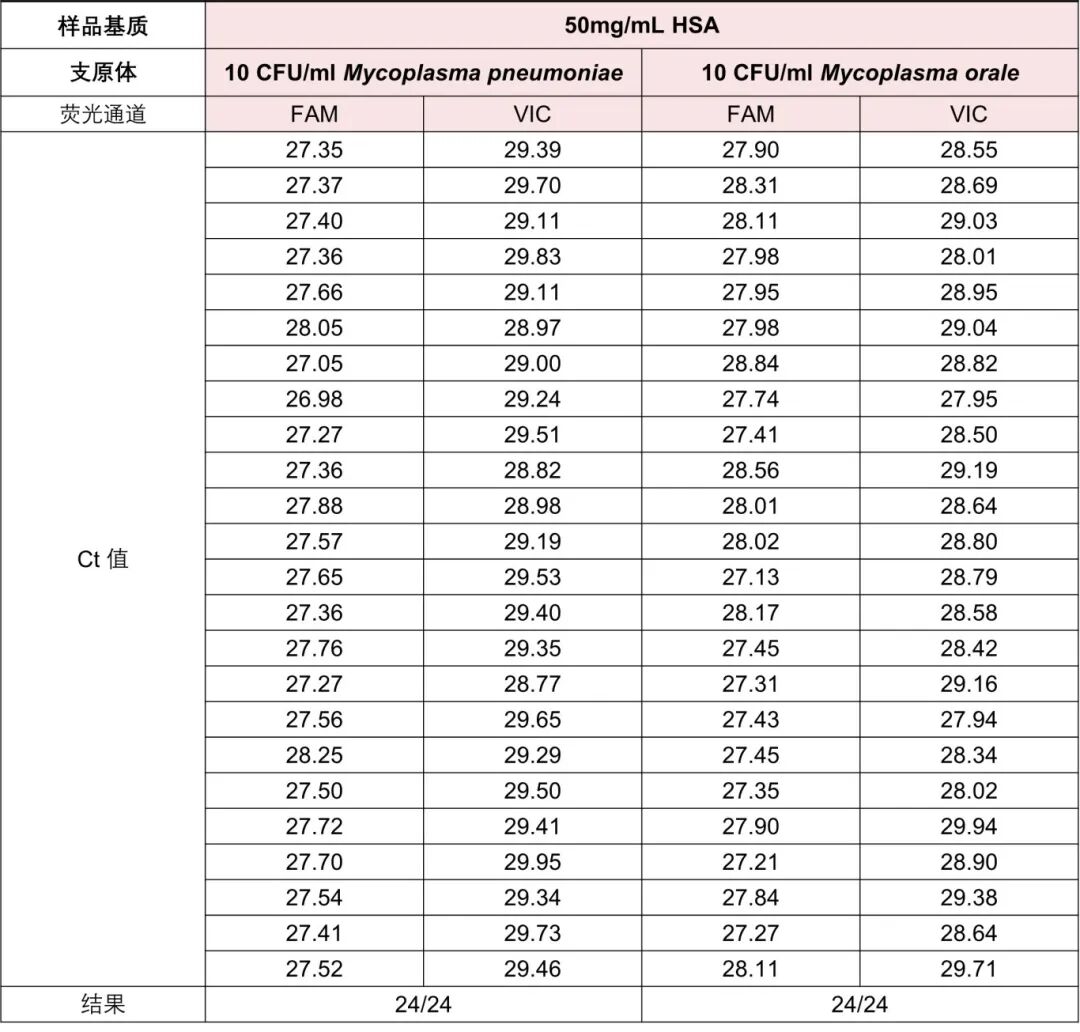
细胞治疗常见基质
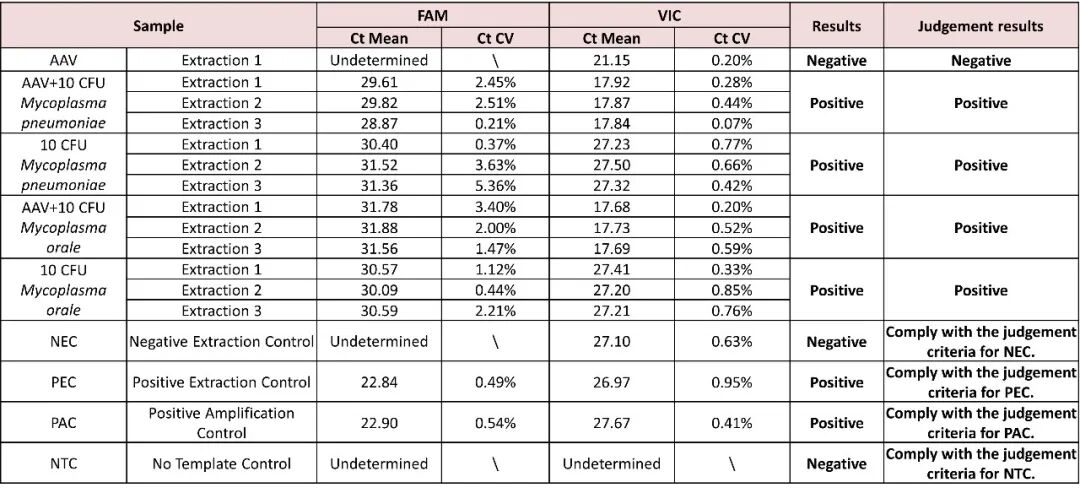
基因治疗样本
-
验证中国、欧洲及美国药典要求支原体菌种,检测灵敏度可达1 CFU/mL
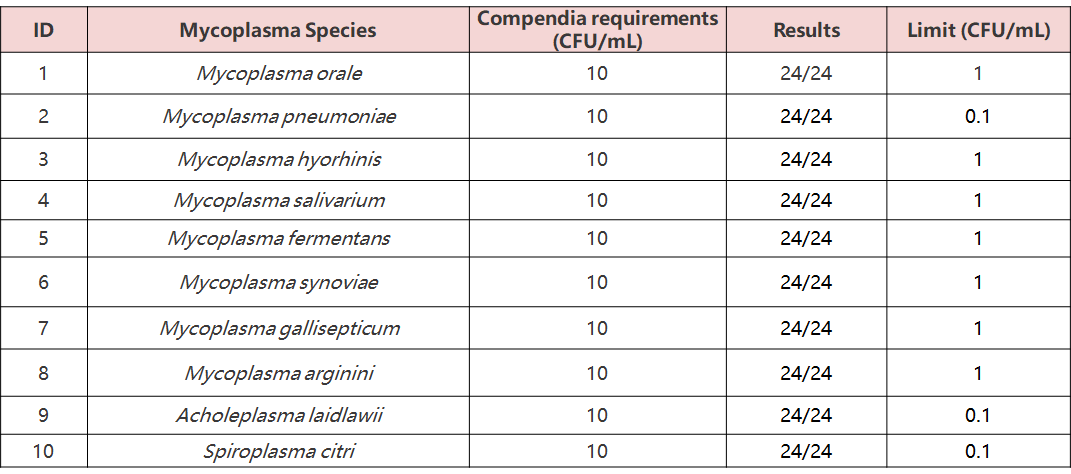
对10个 mycoplasma standards(10 CFU/mL)中的每一个进行24次测试,所有测试结果均为阳性,符合或优于EP 2.6.7的要求(10 CFU/mL)。
-
特异性强,无交叉反应
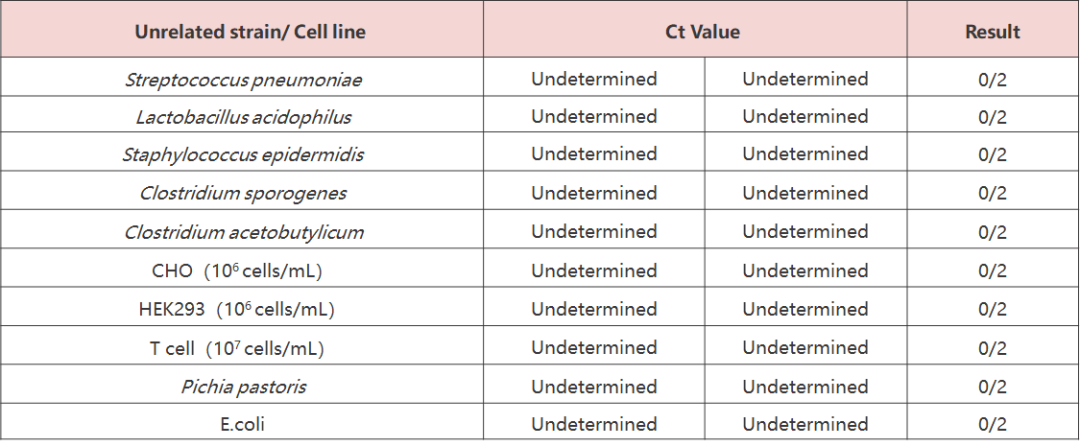
与无关细胞系/菌株的交叉反应:对两种常见细胞系和四种无关菌种进行提取和检测,所有检测结果均为阴性。这表明该试剂盒的支原体检测不受无关细胞/菌株的影响。
-
高品质保证,产品性能优于其他同类产品
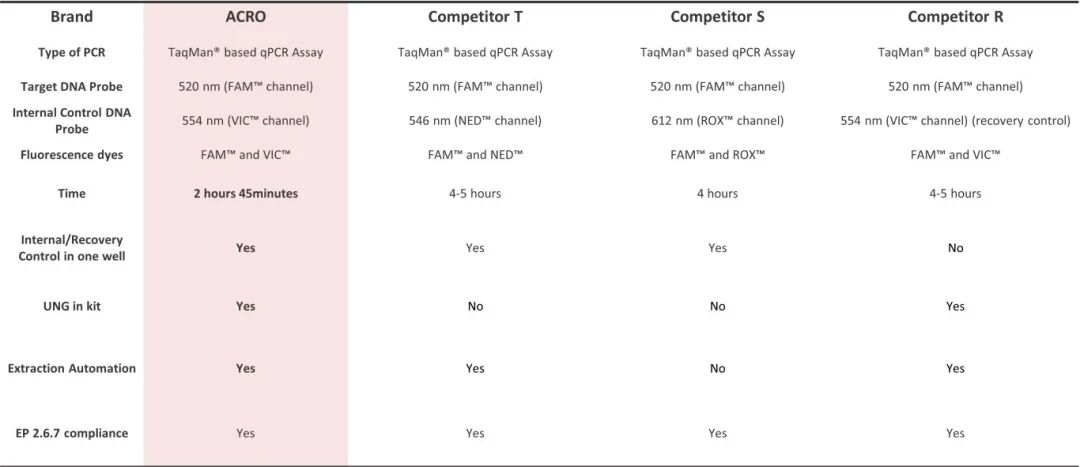
为更好支持方法转移落地,特推出【重组C因子内毒素检测现场DEMO活动】。我们的技术专家将走进您的实验室,通过“上门演示 + 实操指导”的方式,全流程助力您的方法转换与体系验证,为您的内毒素检测开启全新解决方案。

ACROBiosystems
inquiry@acrobiosystems.com
15117918562



