北京百普赛斯生物科技股份有限公司品牌商
14 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
糖尿病功能性治愈大门开启,首-款干细胞胰岛药物上市在即!
1464 人阅读发布时间:2026-03-23 11:14
2月27日,国际学术期刊Lancet Diabetes & Endocrinology在线发表了海军军医大学第二附属医院(上海长征医院)殷浩教授团队联合中国科学院分子细胞科学卓越创新中心程新研究员团队的最-新研究成果:“Autologous and allogeneic stem cell-derived islet therapy in three recipients with type 1 diabetes and complete loss of endogenous pancreatic β-cell function pretransplant”。该项研究是国际上首次分别利用自体与异体干细胞来源的再生胰岛微创移植,实现了3例1型糖尿病患者的胰岛功能重建与血糖自主调控。这一突破不仅标志着糖尿病治疗正式迈入“再生胰岛移植”新纪元,更意味着人类向彻底摆脱供体依赖、规模化治愈糖尿病的终-极目标迈出了关键一步。

传统胰岛移植虽能有效重建血糖稳态:国际数据显示移植后5年完全脱离胰岛素的患者比例已升至60%,其中一例患者维持治愈长达20余年。但其临床应用始终受困于供体胰腺的极度匮乏。面对我国高达1.4亿的糖尿病患者群体,特别是多发病于儿童及青少年的1型糖尿病,这一矛盾尤为尖锐。如何实现胰岛组织的规模化再生,成为全球科学界亟待攻克的世界性难题。
上海长征医院与中科院分子细胞科学卓越创新中心的联合团队,历经十年攻关,成功开发出基于内胚层干细胞(Endoderm stem cell, EnSC)的再生胰岛技术。该技术利用患者自体/健康人供体的PBMC重编程为iPSC,进而建立具有内胚层分化特异性的内胚层干细胞EnSC,并以EnSC为种子细胞在体外制备自体/异体再生胰岛组织(E-islet),该技术通过将干细胞定向诱导分化为功能完备的胰岛样组织,实现了从“等待捐赠”到“按需生产”的根本性转变。这项研究不仅延续了团队此前在治愈2型糖尿病(T2D)领域的重大成果,更在“治愈1型糖尿病”领域迈出了突破性的一步。
基于这一核心技术,团队成功开发了“异体人再生胰岛注射液(E-islet 01)”。这款由健康供体来源的EnSC制备的再生胰岛药物,已于2025年4月和2026年1月先后获得中国国家药监局(NMPA)和美国食品药品监督管理局(FDA)的新药临床试验(IND)批件,成为全球唯-一同时获批中美两国IND的再生胰岛药物。若进展顺利,这一疗法有望在未来5-10年内从临床研究走向常规治疗,彻底改变1型糖尿病的治疗格局。正如《柳叶刀》同期评论所言:“上海长征医院的这项研究,不仅提供了干细胞治疗1型糖尿病的临床概念验证,更以三例患者的详尽数据,揭示了免疫抑制策略与移植物存活之间的关键关联。它向世界证明,干细胞来源胰岛的规模化治疗时代,已经不再遥远。”

扫描添加小助手,了解更多干细胞产品信息!

2026年3月11日至14日,第19届糖尿病先进技术与治疗大会(ATTD 2026)在西班牙巴塞罗那召开。本次会议上,Vertex Pharmaceuticals公司公布了其干细胞衍生胰岛药物Zimislecel(VX-880)的最-新临床研究数据。《Zimislecel(VX-880)在1型糖尿病患者中实现持久血糖控制与消除外源性胰岛素使用》以及《FORWARD研究中接受Zimislecel(VX-880)治疗的1型糖尿病患者达到目标CGM指标》这两项重要报告系统地展示了这款全球进展最快的干细胞胰岛药物的最-新成果。
VX-880是基于同种异体人胚胎干细胞(hESC)来源的完全分化胰岛细胞疗法,其核心技术是将胚胎干细胞在体外定向诱导分化为功能完备的胰岛样组织,这些再生胰岛能够实时感知血糖变化,并精准分泌胰岛素、胰高血糖素等多种激素,从而有效重建血糖稳态。VX-880通过肝门静脉输注的方式移植入患者体内,需要配合免疫抑制方案以防止排斥反应。这一技术路径与上海长征团队的内胚层干细胞(EnSC)路线形成互补,共同推动再生胰岛治疗从实验室走向临床。
根据ATTD 2026公布的最-新数据,VX-880在1型糖尿病患者中展现出前所-未有的疗效。在接受全剂量(0.8×10⁹细胞)单次门静脉输注的患者中,绝大多数患者在随访期内实现了完全胰岛素独立,且这一效果持续稳定。在持续血糖监测(CGM)指标方面,VX-880治疗使患者实现了接近生理状态的血糖控制。安全性方面,VX-880显示出良好的耐受性。多数不良事件为轻至中度,主要包括腹泻、头痛、恶心等,主要与免疫抑制方案相关,而非细胞产品本身。研究中未出现与VX-880直接相关的严重不良事件或死亡。
Vertex公司在会上宣布,VX-880的III期临床试验(FORWARD研究)进展顺利,已于2025年上半年完成患者入组和给药,计划在2026年向全球多个国家的监管部门递交上市申请。该产品此前已获得美国FDA的“再生医学先进疗法”(RMAT)认定与快速通道资格,以及欧洲EMA的“优先药物”(PRIME)认定。据悉,其三期临床试验预计将在2026年6月完成,有望于2026年年底正式上市。若如期获批,这将是全球首-个上市的干细胞衍生胰岛药物,彻底改变1型糖尿病的治疗格局。
目前,全球范围内已有三个研究团队成功实现1型糖尿病的功能性治愈,其中两个来自中国——程新/殷浩团队与邓宏魁/沈中阳团队,另一个则是美国的Melton/Vertex公司团队。对于数百万1型糖尿病患者而言,2026年有望成为历史性的一年——首-款干细胞胰岛药物的上市,将标志着糖尿病治疗正式从“胰岛素替代”迈向“细胞治愈”的再生医学新纪元。
ACROBiosystems百普赛斯凭借强大的细胞培养平台,在严格的GMP质量管理体系下自主研发的Activin A、KGF、Betacellulin(BTC)、FGF basic等产品旨在支持大规模的干细胞向内胚层的分化,包括β胰岛细胞及其他细胞类型。凭借稳定的产品工艺,目前已助力多家iPSC企业开发iPSC到T/NK等免疫细胞、功能性胰岛细胞、神经细胞、心肌细胞、视网膜上皮细胞等工艺,并成功用于临床生产中。同时,作为细胞治疗领域创新解决方案的提供者,公司依托具有完全自主知识产权的先进AI蛋白质设计平台,通过对热稳定蛋白和高活性蛋白的改造,帮助客户实现更稳健、规模可放大且成本可控的生产工艺,目前已推出AI改造的FGF basic和Activin A等产品,进一步加速iPSC疗法的研究与转化进程。
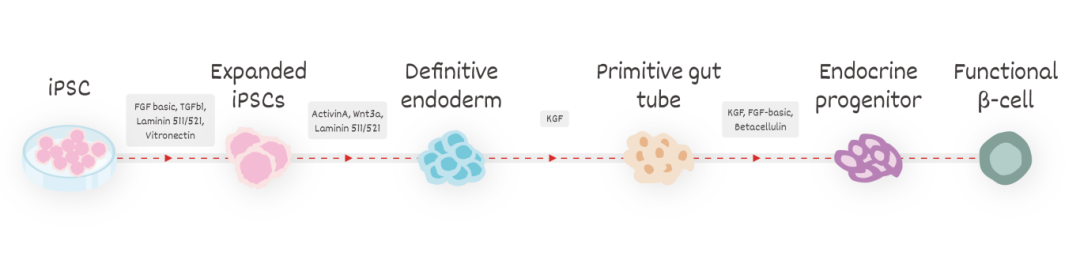
ACROBiosystems百普赛斯在iPSC-胰岛分化过程中可提供的产品
-
GMP级Activin A促进内胚层分化

Activin A (Cat. No. GMP-ACAH37) could effectively induce the endoderm differentiation by FOXA2 and SOX17 expression in immunofluorescence and FACS.
-
GMP级KGF促进胰腺祖细胞分化

KGF (Cat. No. GMP-FG7H35) could promote iPSC differentiation into pancreatic progenitor cells, with high expression of PDX1 and SOX9.
-
Activin A、KGF、BTC等联合作用,高效诱导iPSC分化为功能性成熟胰岛细胞
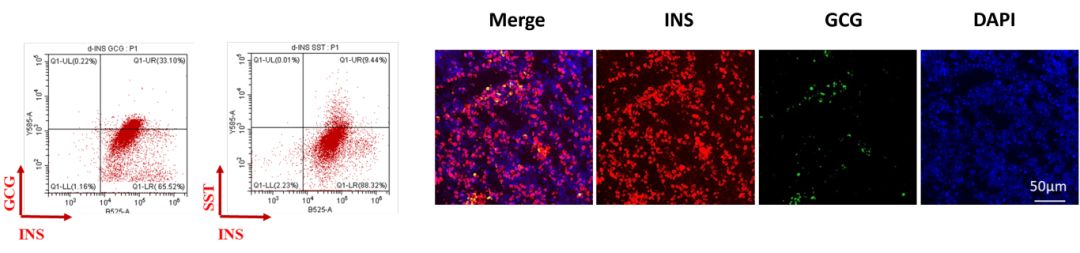
Activin A (Cat. No. GMP-ACAH37), KGF (Cat. No. GMP-FG7H35), FGFb (Cat. No. GMP-FGCH17) and Betacellulin (Cat. No. BEN-H5116) coating with Laminin 521 (Cat. No. GMP-LA5H24) could promote iPSC differentiation into mature islet cells in 32 days with the composition of insulin - producing beta cells, glucagon - secreting alpha cells marked by GCG, and HEK - derived delta cells marked by SST, optimized to replicate native islet function for effective glucose regulation.
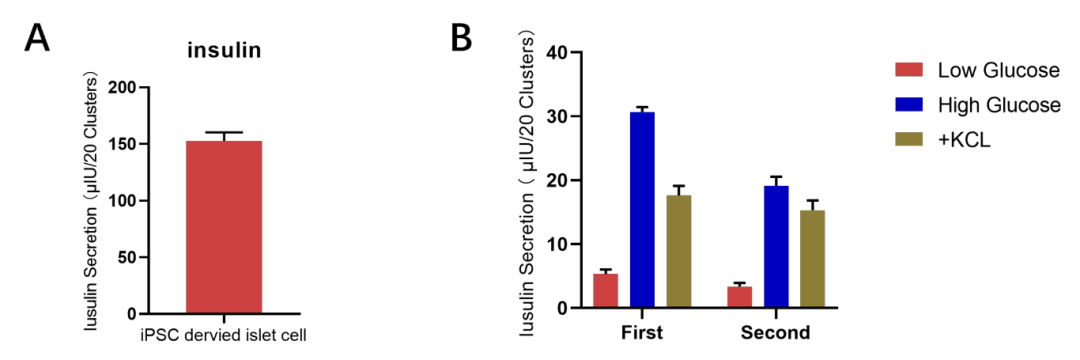
(A) Insulin secretion of islet cells after 35 days of differentiation. (B) Glucose-stimulated insulin secretion of islet cells differentiation. Islets differentiated for 35 days exhibit detectable secretory function, as confirmed by a glucose stimulation assay which demonstrates their fundamental glucose-responsive capability.

以上产品均正在开启限时试用装活动,扫描下方二维码立即申请!


ACROBiosystems
inquiry@acrobiosystems.com
15117918562
(备注:姓名+公司)



